Theorie der Massenspektrometrie - Teil 1
Innerhalb dieses Kurses zur Flüssigkeitschromatographie gekoppelten Massenspektrometrie (LC-MS) sollen neben theoretischem Wissen und Hilfestellungen mit einigen Tipps für Ihre eigene LC-MS Analytik auch nützliche Hinweise für die Erstellung sowie Optimierung einer Messmethode vermittelt werden. Ein weiterer Schwerpunkt liegt im Bereich des Troubleshootings.
Der Inhalt besteht aus insgesamt 6 Kapiteln bzw. Modulen, die jeweils im Wochentakt freigeschaltet werden. Im Anschluss an das sechste Kapitel, wird das vermittelte Wissen durch einen kurzen Abschlusstest verifiziert. Nachdem Sie alle Module sowie den Test erfolgreich abgeschlossen haben, erhalten Sie nach Ablauf der Prüfungsfrist ein Zertifikat für diese Schulung.
1 - Theorie der Massenspektrometrie - Teil 1
2 - Theorie der Massenspektrometrie - Teil 2
3 - Troubleshooting: Was mache ich bei hohem Hintergrundrauschen?
4 - Troubleshooting: Welche Möglichkeiten habe ich bei Sensitivitätsverlust?
5 - Methodenoptimierung: Quellenoptimierung
6 - Methodenoptimierung: MRM-Optimierung
Beginnen wir zunächst mit einem kurzen Theorie Teil über die Massenspektrometrie. Dieses Kapitel ersetzt dabei kein Lehrbuch, sondern soll lediglich einen kurzen Überblick über die Thematik verschaffen. Für weitere Informationen empfehlen wir den Shimadzu Fundamental Guide LCMS.
HPLC-gekoppelte Massenspektrometrie (LC-MS)
In der modernen instrumentellen Analytik ist die Massenspektrometrie nicht mehr wegzudenken. Durch dieses Analyseverfahren können sowohl qualitative als auch quantitative Bestimmungen verschiedener Atom- oder Molekülmassen durchgeführt werden. Dabei finden sich die unterschiedlichsten Einsatzmöglichkeiten. Von der klinischen Diagnostik zur Detektion von Biomarkern oder der Bestimmung von Arzneimittelspiegeln im Blut über Qualitätskontrollen von Syntheseprodukten bis hin zu der Untersuchung von Gewässern und Lebensmitteln bezüglich Pestizide oder Hormone.
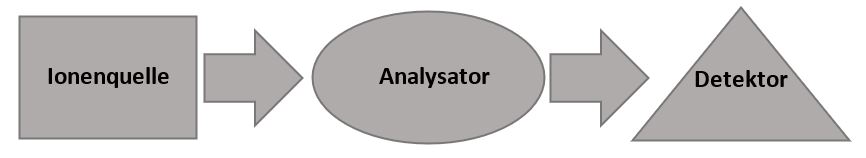
Abb. 1: Schematischer Aufbau eines Massenspektrometers
- Eine Ionenquelle dient der Ionisierung und zur Überführung der Analyten in die Gasphase.
- Der Analysator ist das Herzstück des Massenspektrometers, um die Ionen nach ihrem Masse-zu-Ladungs-Verhältnis (m/z) zu separieren.
- Der Detektor erfasst die auftreffenden Ionen, verstärkt die Signale und leitet die Informationen an eine Datenstation (bspw. PC) zur Aufzeichnung der Ergebnisse und letztlich für die Auswertung weiter.
Ionenquellen
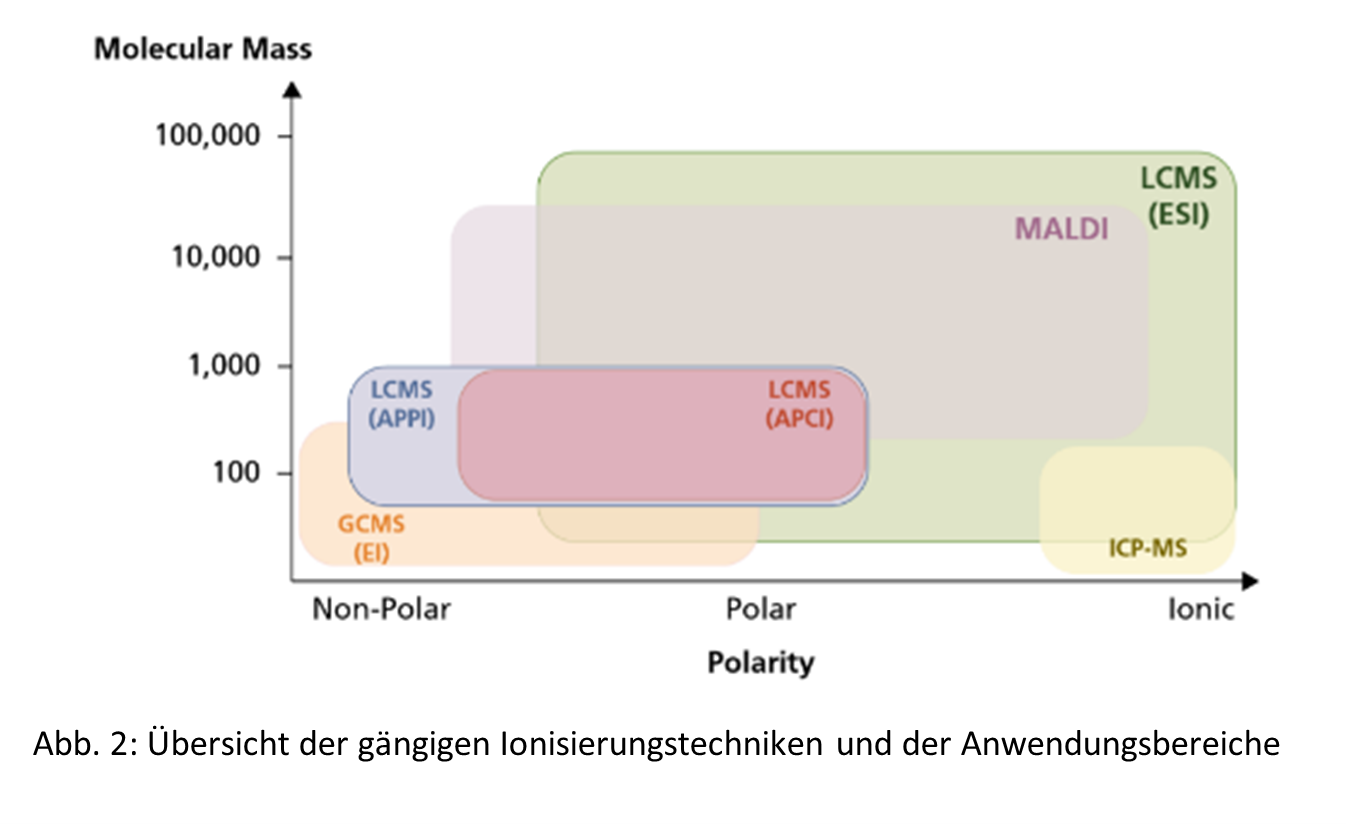
Es stehen eine Vielzahl an Ionisierungs-Technologien zur Verfügung. Die Auswahl der Ionenquelle ist dabei abhängig von dem zu untersuchenden Probenmaterial und der jeweiligen Fragestellung. Dabei spielen viele Parameter, vor allem der Polaritätsbereich, die Molekülgröße der Analyten und die Komplexität des Probenmaterials eine wichtige Rolle.
ESI – Electrospray Ionization
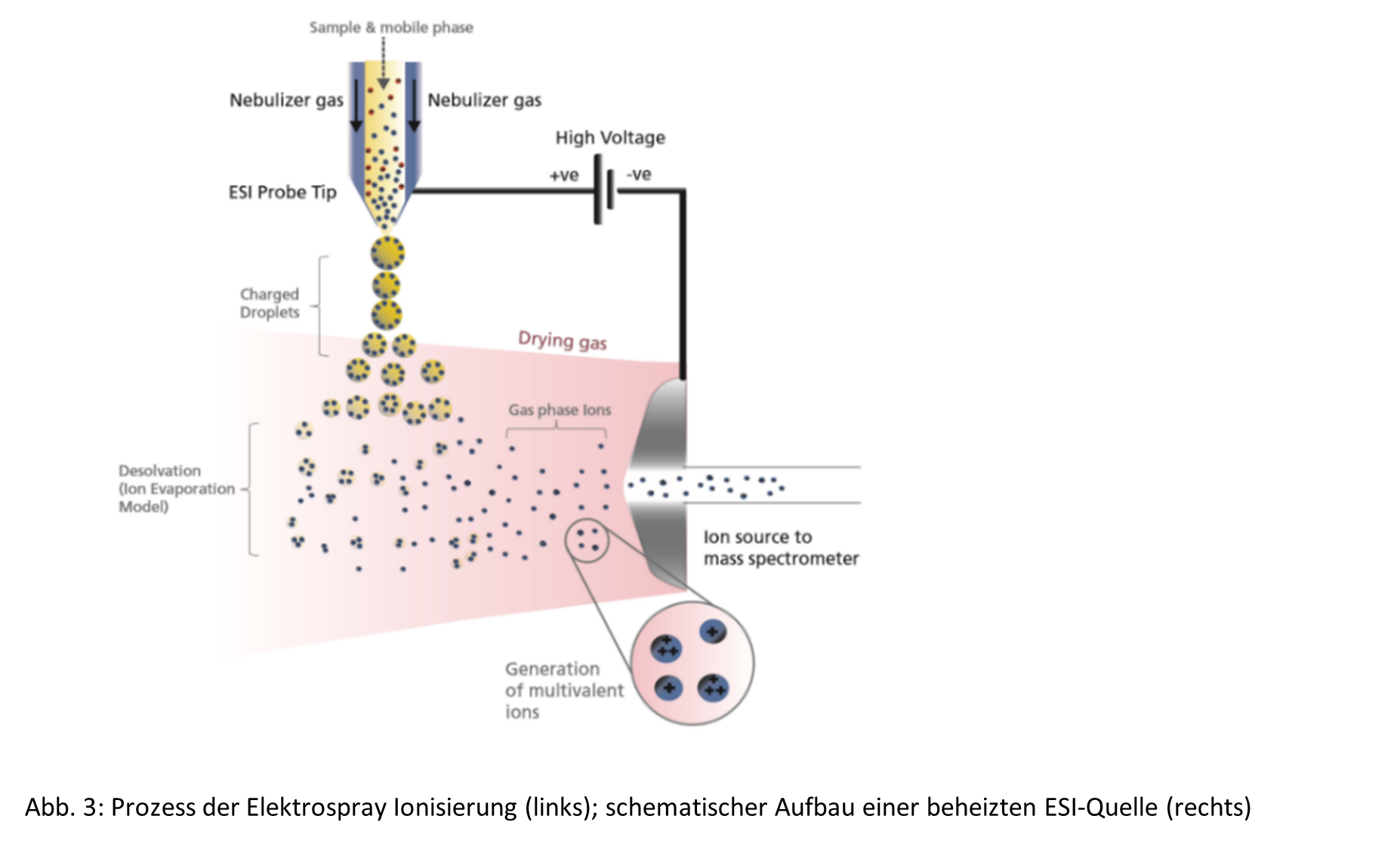
Bei dem Verfahren der Elektrospray Ionisierung wird ein sehr feiner Nebel von der eingebrachten Probenlösung (durch z.B. einer HPLC oder eine Spritzenpumpe) an der Spitze der ESI-Kapillare erzeugt. Für die Ionisierung der Analyten wird an dieser ESI-Kapillare eine hohe elektrische Spannung im Bereich von 3 bis 5 kV angelegt. Diese sorgt zunächst für eine Akkumulation von Ladungen auf der Tröpfchenoberfläche des Flüssigkeitssprays. Zusätzlich wird zur Unterstützung der Lösemittelverdampfung ein sogenanntes Nebulizing Gas, welches parallel neben der ESI-Kapillare bzw. des ESI-Sprays in die Quelle eingeleitet wird. Oftmals wird hier zusätzlich ein weiteres Heizgas in der Quelle genutzt, um die Verdampfung und so die Ionisierung zu steigern. Aufgrund der Lösemittelverdampfung kommt es zu einer Oberflächenverkleinerung der Flüssigkeitströpfchen mit einhergehender Verdichtung der akkumulierten Ladungen. Letztlich erzielen wir die Übertragung von Ladungen auf die einzelnen Analyten durch einen als Coulomb Explosion bezeichneten Vorgang. Nach dem hier dargestellten Model wird beschrieben, dass sich dieser Vorgang mehrfach wiederholt und somit immer kleinere Tröpfchen entstehen, die in die Gasphase übergehen bis schließlich nur die einzelnen Ionen übrigbleiben. Der ESI-Prozess beschreibt eine weiche Ionisierung, wodurch wenig bis keine Fragmentierung der Moleküle in der Quelle entstehen.
APCI – Atmospheric Pressure Chemical Ionization
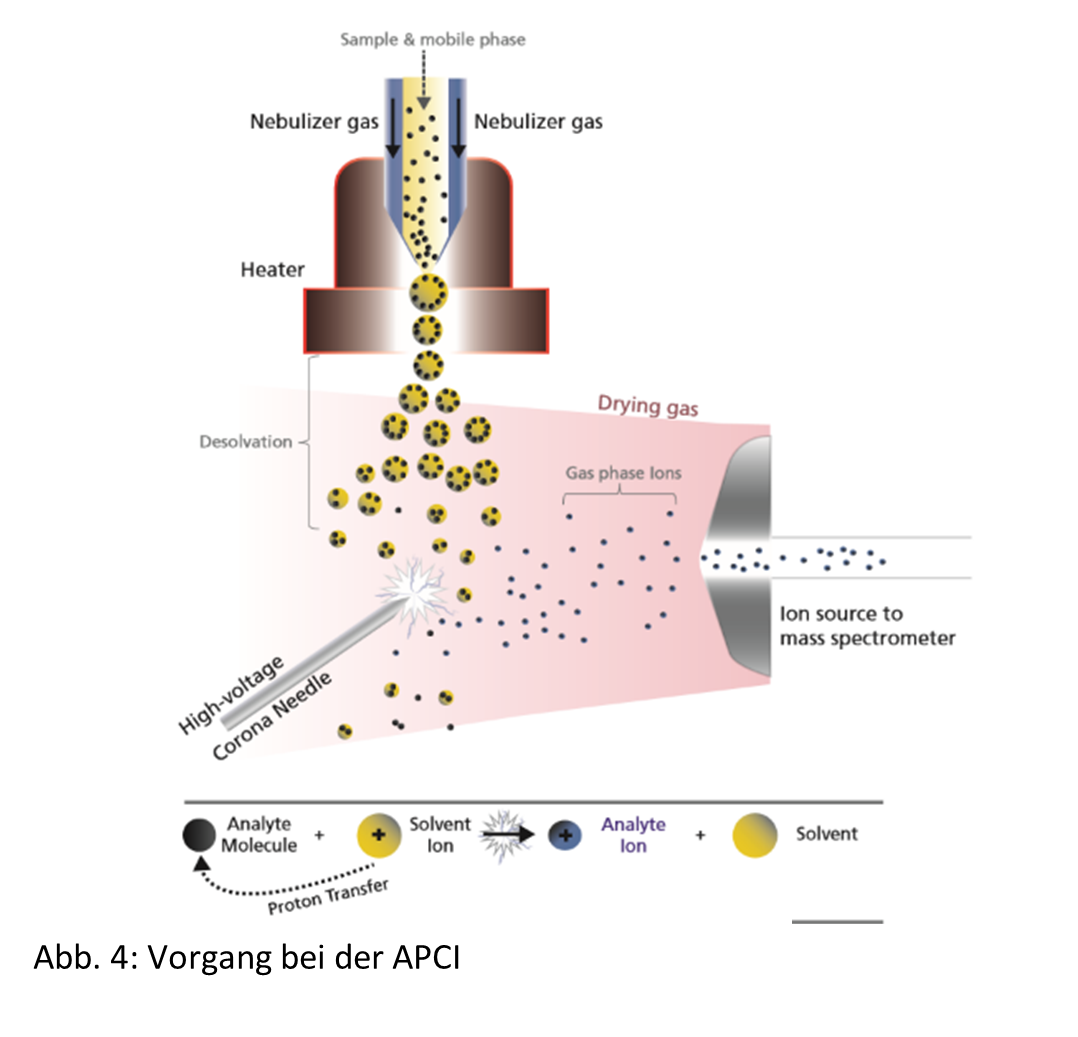
Der Aufbau einer APCI-Quelle ähnelt dem einer ESI-Quelle. Das Prinzip ist in der folgenden Abbildung dargestellt.
Hauptsächlich kommt die APCI-Quelle und die hier verwendete chemische Ionisierung bei der Analytik von kleineren und wenig oder mittelpolaren Analyten zum Einsatz. In der APCI-Quelle werden Lösemittel sowie Probenlösung durch sehr hohe Temperaturen und Hilfsgase wie Stickstoff (Nebulizing Gas) in die Gasphase überführt. Mittels der Corona-Nadel und der hier anliegenden Hochspannung werden zunächst überwiegend die Gas- und Lösemittel-Moleküle ionisiert. Die Ladungen werden anschließend in mehreren teils radikalischen Reaktionsschritten auf die Moleküle der Analyten übertragen. Im Unterschied zur ESI-Ionisierung entstehen bei der APCI, aufgrund der größeren Distanz einzelner Moleküle im Gasgemisch, überwiegend einfach geladene Ionen.
Quadrupol:
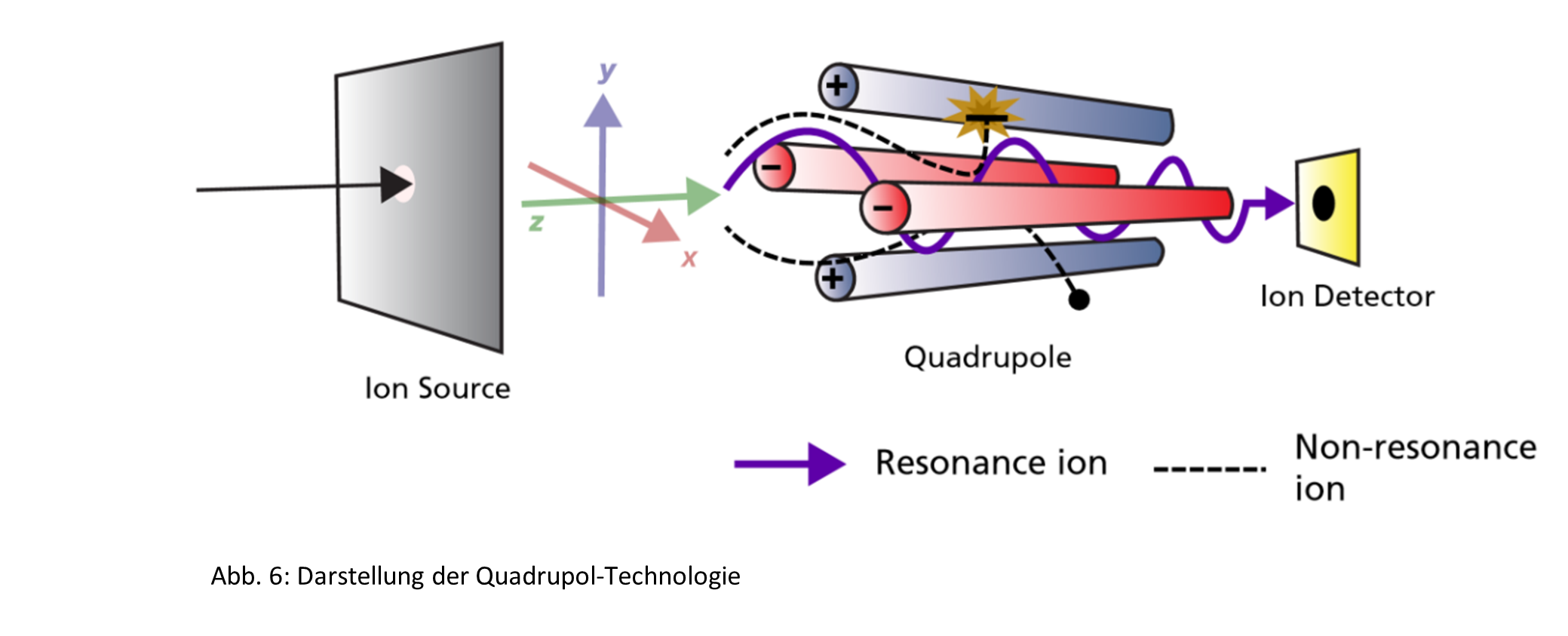
Ein Quadrupol besteht, wie der Name bereits verrät, aus vier parallel angeordneten zylindrischen Metallstäben. Am Quadrupol werden sowohl eine Gleichspannung in Flugrichtung der Ionen als auch eine hochfrequente Wechselspannung oder Radiofrequenz zwischen den einzelnen Stäben angelegt. Dabei ist die Polarität der Wechselspannung bei den jeweilig gegenüberliegenden Quadrupolstäben im Wechsel identisch. Je nach Abstimmung von Gleich- und Wechselspannung im Quadrupol können Ionen definierter m/z-Werte den Quadrupol passieren oder werden aufgrund von unstabilen Resonanzen aussortiert. Ob sich die Ionen in dem Feld des Quadrupols stabil verhalten oder nicht, wird durch die Mathieu-Gleichung beschrieben:
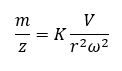
m: Masse des Ions
z: Ladungszustand
K: Konstante
V: Angelegte Spannung
r: Effektive Distanz zwischen Elektroden
ω: Schwingungsfrequenz
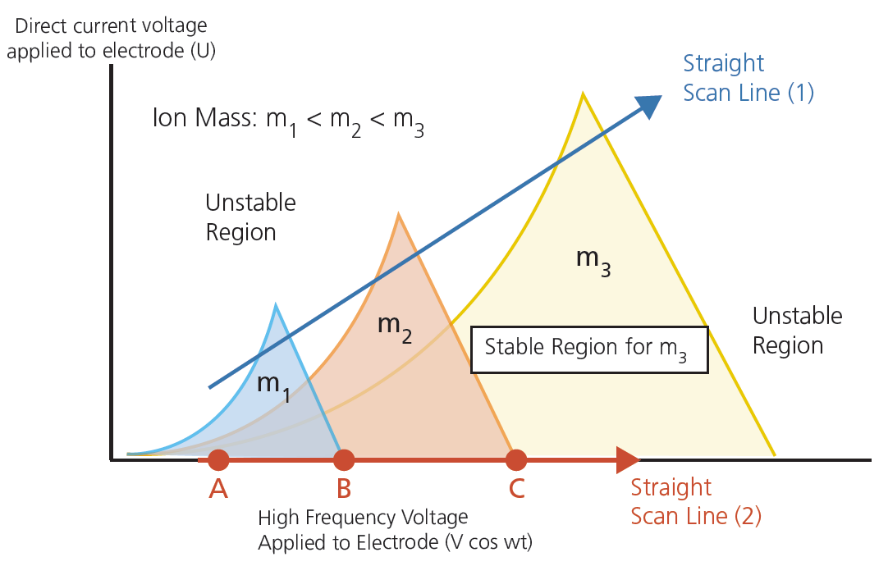
Abb. 7: Grafik der stabilen Felder im Quadrupol
Wie in der Abbildung zu sehen, können die Ionen innerhalb einer stabilen Oszillation den Quadrupol passieren. Jedoch für Ionen mit anderen m/z-Werte sorgen die so eingestellten Spannungswerte des Quadrupols für ein unstabiles Feld bzw. eine unstabile Flugbahn. Dadurch werden diese Ionen „ausgefiltert“ und können den Detektor nicht erreichen. Durch eine schnelle Änderung der Einstellungen am Quadrupol im Millisekunden-Bereich können viele Spannungen nacheinander geschaltet oder die Spannung als Rampe angelegt werden. Mittels dieser Technologie kann der Analysator bestimmte voreingestellte Ionen selektiv filtern oder gewählte Massenbereiche analysieren.
TOF (Time of Flight) – Flugzeitmassenspektrometer:
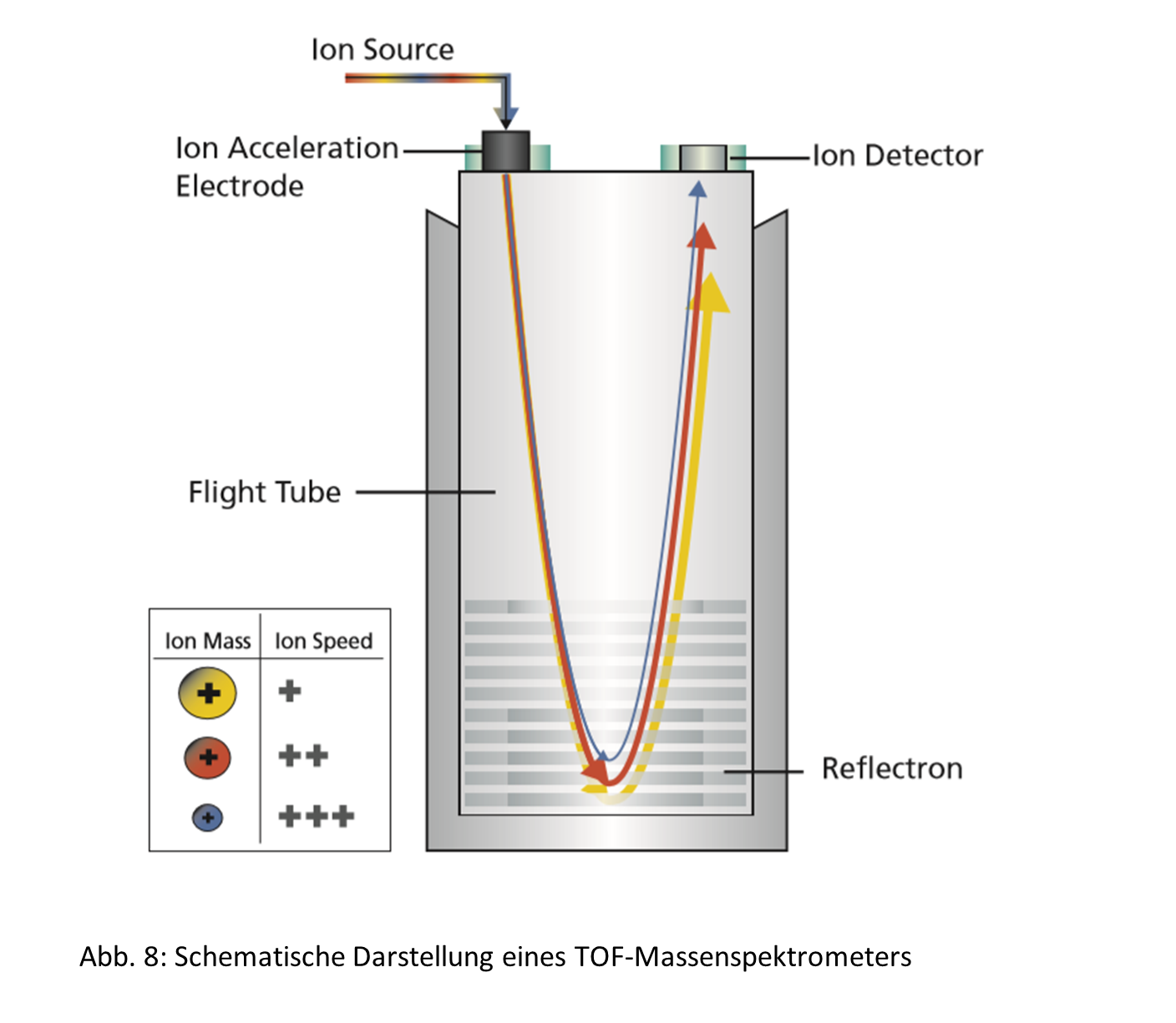
Bei der massenspektrometrischen Analyse mittels TOF-MS werden die Ionen in ein feldfreies Flugrohr geleitet. Aufgrund der unterschiedlichen Flugzeiten der Ionen, je nach Größe, werden diese voneinander separiert.
Nach der Ionisierung der Analyten in der Ionenquelle werden die Ionen zunächst durch eine sogenannte Ionenoptik geleitet. Diese dient der Vorselektion eines Massenbereiches und der Fokussierung. Anschließend werden die Ionen mittels hoher angelegter elektrischer Spannung beschleunigt und in eine feldfreie Driftstrecke überführt. Die so auf die Ionen übertragene kinetische Energie führt zu einer spezifischen Flugzeit der Ionen, die von Ihrem jeweiligen Masse zu Ladungsverhältnis (m/z-Wert) abhängig ist. So erreichen Moleküle mit kleineren m/z-Werten den Detektor früher als Moleküle mit größeren m/z-Werten. Durch diese Eigenschaften des TOF-MS werden hochaufgelöste Spektren mit hoher Massengenauigkeit generiert. Einen weiteren Vorteil der TOF-Systeme bietet der hohe mögliche Massenbereich der Analyse. Allerdings benötigt ein solches System eine äußerst stabile Temperierung, da minimale Unterschiede in der Flugstrecke sich unmittelbar auf die Massengenauigkeit auswirken.
Ionenfalle
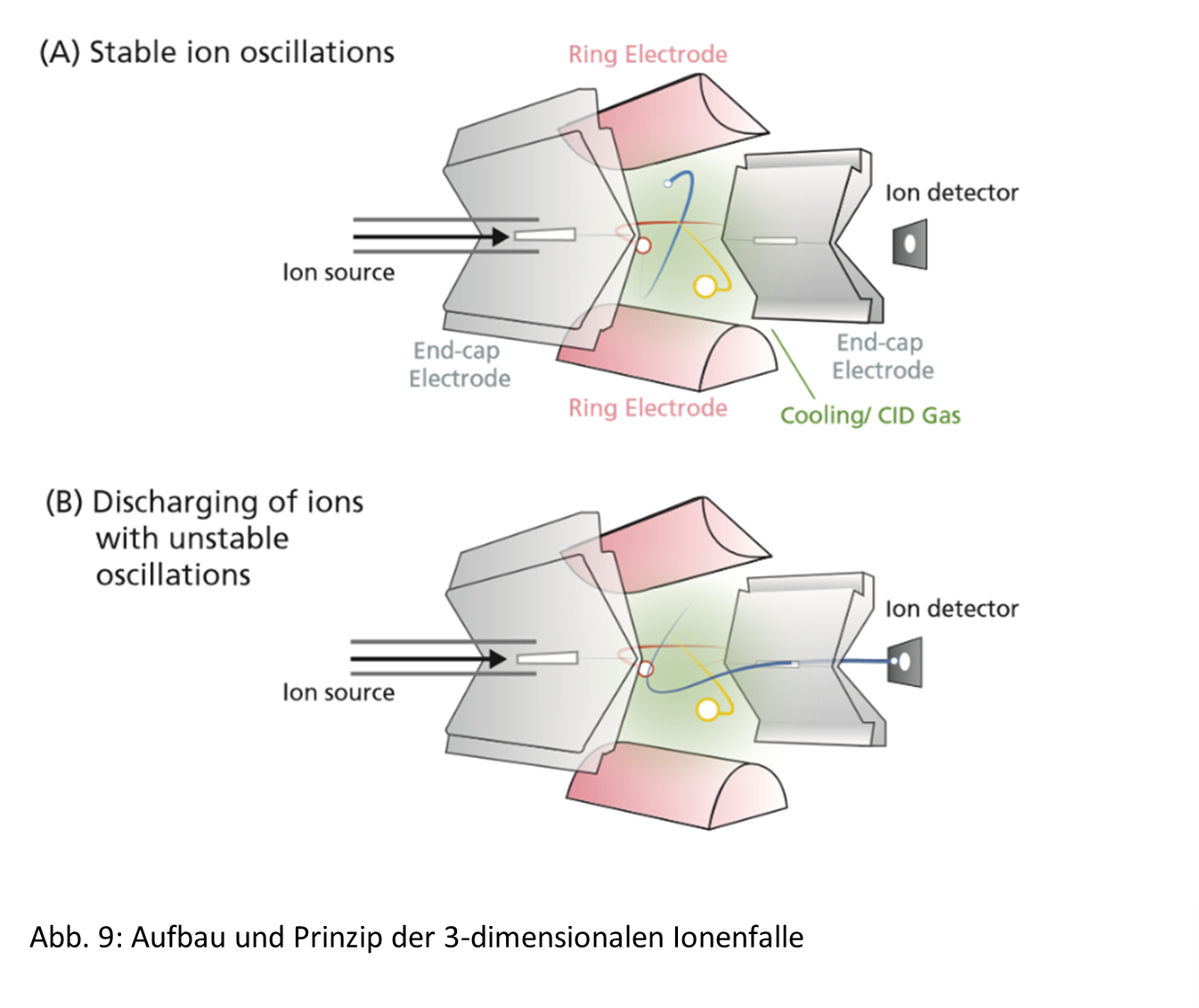
Die Technik der Ionenfalle gibt es in unterschiedlichen Bauformen. Zum einen als 2-dimensionale lineare oder als 3-dimensionale ringförmige Ionenfalle. Das Prinzip der Ionenfalle verläuft, ähnlich der Quadrupol-Technologie, ebenfalls nach der Mathieu-Gleichung. Der Aufbau einer Ionenfalle ist in der Abbildung 9 dargestellt. Um ein Spektrum aufzunehmen, werden zunächst End-Cap und Ringelektrode geerdet und die Ionen pulsiert in die Falle eingeführt. In der Falle werden Ionen dann durch eine angelegte hochfrequente Wechselspannung zentralisiert und so in der Falle „gefangen“. Anschließend können die Ionen durch sukzessive Reduktion der Wechselspannung an der Ringelektrode und durch eine angelegte Gleichspannung an den End-Cap Elektroden aus der Ionenfalle ausgeschleust und detektiert werden.
Um ein spezifisches Ion zu detektieren, wird bei angelegter Wechselspannung an der Ringelektrode nun auch eine, auf den relevanten m/z-Wert abgestimmte, Wechselspannung an den End-Cap Elektroden angelegt. Die Detektion des isolierten m/z-Wertes geschieht, wie bei der Analyse des kompletten Spektrums, wiederum durch Wegnahme der Wechselspannung und dem Anlegen einer Gleichspannung an den End-Cap Elektroden. In der Abbildung 9 sehen wir, wie das blau dargestellte Ion durch die veränderten Spannungswerte seine stabile Flugbahn verliert und durch die Öffnung an den End-Cap Elektroden die Ionenfalle verlässt. Neben den Vorgängen des Einfangens und der Ausschleusung, ermöglicht die Ionenfalle zudem eine Fragmentierung definierter m/z-Werte. Hierzu wird ein zusätzliches Stoßgas in die Ionenfalle eingeleitet, dass nach dem Vorgang des Einfangens, ebenfalls durch hochfrequente Wechselspannung angeregt, eine effiziente Stoßfragmentierung vermittelt. Die durch Kollision mit dem Stoßgas erzeugten Fragmente der Analyten (MS2-Fragmente) lassen sich nun entweder am Detektor auslesen oder entsprechend weiter fragmentieren.
Diese sogenannten MSn-Analysen eignen zur Untersuchung unbekannter Verbindungen beispielsweise bei Fragestellungen rund um die Struktur und den Aufbau eines Moleküls.
Detektoren
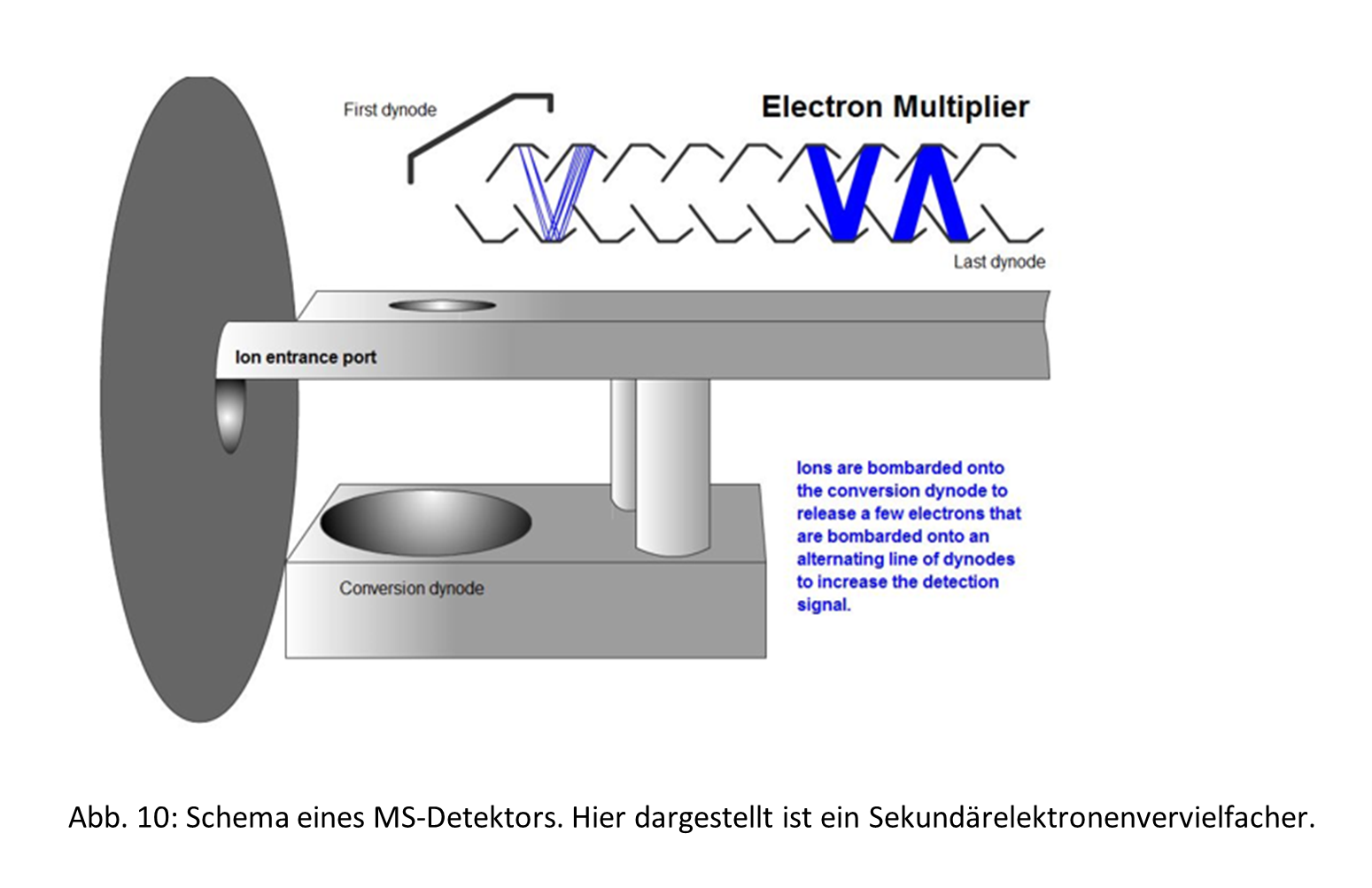
Für gewöhnlich werden Sekundärelektronenvervielfacher oder Microchannel Plates (MCP) als Detektoren in der Massenspektrometrie eingesetzt. Die Ionen treffen bei einem Sekundärelektronenvervielfacher zunächst auf die sogenannte Konversionsdynode. Aus dieser werden durch den Aufschlag eines Ions Elektronen freigesetzt, die anschließend in einem Sekundärelektronenvervielfacher (Elektron Multiplier) in ein messbares Signal verstärkt werden. Diese Signale werden letztlich auf dem Messrechner bzw. in der entsprechenden Software ausgegeben.


